- Katılım
- 22 Ağu 2018
- Konular
- 147
- Mesajlar
- 555
Daha fazla
- Adım
- basri
- Cinsiyet
- Erkek
- Cihaz
- iPhone 11 pro
Kimya, maddenin yapısını, özelliklerini, bileşimini, etkileşimlerini ve tepkimelerini araştıran bilim dalıdır.[1][2] Kimya bilimi daha kapsamlı bir ifadeyle, maddelerin özellikleriyle, maddelerin sınıflandırılmasıyla, atomlarla, atom teorisiyle, kimyasal bileşiklerle, kimyasal tepkimelerle, maddenin hâlleriyle, Moleküller arası ve moleküller kuvvetlerle, kimyasal bağlarla, tepkime kinetiğiyle ve kimyasal dengenin prensipleriyle ve benzeri konullarla ilgilenir. Kimya'nın ana alt bilim dalları, analitik, anorganik, organik kimya ve fizikokimya dır.
Kimya köken bilimi
Kimya sözcüğüyle simya sözcüğünün aynı kökten geldiği tahmin edilmektedir. 17 yüzyılda kimya ve simya sözcükleri aynı bilimsel disiplini, (maddenin analizi, sentezini içeren çalışmaları) tanımlamak için ayırt edilmeksizin kullanılmışlardır. Ancak 18. yüzyılda bu iki sözcük arasında bir ayrım gözetilmeye başlanmış, simya daha çok metalden altın yapmakla ilgili uğraşları tanımlamak için kullanılmıştır.[3] Simya sözcüğünün Arapça al-kimia (الكيمياء‎ sözcüğünden türediği[4], bu Arabça sözcüğünde Antik Yunanca himya (metal eritmek alnamına gelen χημεία ya da χημία sözcüğünden türediği idda edilmektedir
Tarih
Kimya'nın tarihi Simya öncesi, Simya dönemi, Geleneksel ve Modern kimya dönemleri olmak üzere 4 ana başlık altında toplanarak incelenebilinir.
Simya öncesi
Kimyanın bilinen tarihi Antik Mısır döneminde başlamıştır. MÖ 2000'li yıllarda Mısırlılar'ın kimyasal yöntemler kullanarak kosmetik tozlar ürettikleri idda edilmektedir.[6] Kral Hamurabi döneminde (MÖ 1792-1750) Babiller altın, gümüş, civa, kurşun, demir ve bakır gibi metalleri tanımlanmış ve bu metallere semboller verilmiştir.[7] Erken Yunan felsefeciler (Sokrates öncesi düşünürler) doğal olayları doğaüstü olmayan nedenlerle açıklamaya çalışmışlar[8], bunun sonucunda da bu dönemde simya öncesi kimya biliminin temelleri atılmıştır. Miletli Tales (MÖ 624 MÖ 546) maddenin presiplerini araştırmış ve suyun evrenin temel maddesi olduğunu öne sürmüştür.[9] Bir diğer Miletli Anaksimandros (MÖ 610- MÖ 546) suyun karşıtı olan ateşin nasıl oluştuğunu sorgulamıştır.[10] Empedokles (MÖ 490-430) evrenin 4 temel element ateş, hava, su ve topraktan oluştuğunu idda etmiştir.[11] Empedokles'in tanımına göre toprak katı maddeleri, su sıvı maddeleri ve metalleri, hava gasları ifade etmekteydi. Bununla beraber ateşide bir süreçten çok sıvı,gaz ve katı gibi maddenin bir hali olarak tanımlamıştır. Demokritos'un hocası Leukippos evrenin iki çeşit elementten oluştuğunu (boşluk ve katı) ifade etmiş, boşluğun ve katılığın evrendeki tüm elementleri oluşturduğunu ifade etmiştir.[12] Democritus (MÖ 460-370 ) Leukippos ile birlikte atomcu teoriyi geliştirmiştir.[13] Maddelerin yapı taşı olarak daha küçük parçalara ayrılamayan atomlar Leucippus ve Democritus'un geliştirdiği bir felsefe sistemi olarak kabul edilmesine rağmen Platon bu atomculuk teorisine bölünemezlik prensibini eklemiştir. Plato evreni oluşturan 4 temel elementin geometirik katılardan oluştuğunu bu katılarında üçgen yüzeylerden oluştuğunu idda etmiştir.[14] Aristoteles (MÖ 384-323) elementlerin özellikleri düşüncesini geliştirmiştir. Farklı elementlerin farklı özellikleri olduğunu ve bunun çeşitli nicel değişkenlere bağlı olduğunu ifade etmiştir. Bu nicel özellikleri değiştirildiğinde bir elementin başka bir elemente dönüştürülebileceğini ve maddelerin değişim halinde olduğunu idda etmiştir.
Simya dönemi
Aristotalesin fikirlerinden etkilenen simyacılar (yaklaşık MÖ 320, MS 300) yılları arasında Yunanca konuşulan akdeniz kıyılarında, Mısır'da, İran'da Aristotales ve diğer Yunan filozofların teorilerini pratiğe geçirmeye başlamışlardır.[16][17] Yine bu dönemde ilk defa simyacılar ucuz metallerden altın elde etmeyi mümkün kılması düşünülen felsefe taşını üretmeye çalışmışlardır.[7]
13. yüzyıla gelindiğinde simya tüm Avrupa kıtasında yaygın bir hale gelmiş, örneğin dönemin önemli bilim adamlarından Raymundus Lullus[18] İngiltere kralı tarafından İngiltere'ye basit metalden altın üretmesi için davet edilmiştir.[7] 13. yüzyılın başlarında dönemin ünlü simyacıları Roger Bacon[19] (1214/12201292), Albertus Magnus[20], ve Raymundus Lullus basit metalden altın üretme yöntemleri dışında simyanın diğer alanlarına yönelip, simyanın günümüz kimyasına yaklaşmasına öncü olmuşlardır.[21]
14. yüzyılda Katolik Kilisesi simya karşıtı taraf olmuş ve 1317 yılında Papa John XXII simyacılığı yasaklamıştır.[22]
17. yüzyıla gelindiğinde simya göreceli olarak az da olsa hala varlığını sürdürmekteydi. 17. yüzyılın etkin bilim adamlarından Robert Boyle 1661 yılında döneminde büyük yankı uyandıran eseri The Sceptical Chymist'i yayımlamıştır.[23] Aristotales'in 4 element teorisini ret eden bu kitap aynı zamanda simyanın döneminin de sona erdiğini işaret etmekteydi.[24]
Simya döneminde simyacıların araştırmaları ve deneyleri vasıtasıyla birçok laboratuvar tekniği geliştirilmiş ve çeşitli bileşik ve elementler keşif edilmiştir
Geleneksel kimya
Bu dönem 17. yüzyıl sonuyla 19. yüzyıl başlarına denk gelmektedir. Johann Joachim Becher 17. yüzyıl ortalarında yanma ile ilgili Phlogiston teorisini geliştirmiştir. Bu teoriye göre her yanıcı madde phlogiston diye adlandırılan kokusuz, renksiz, tatsız ve ağırlıksız bir içerik içermekteydi ve bu içerik yanma gerçekleştiğinde yanıcı madde tarafından ortama salınmaktaydı.[25]
Bu teori daha sonra Georg Ernst Stahl tarafından daha popüler bir hale getirilmiş 18. yüzyılın büyük bir kısmında genel kabül görmüştür.[26] 1785 1787 yılları arasında Fransız fizikçi Charles Augustine de Coulomb günümüzde Coulomb yasası olarak adlandırılan benzer yüklü maddelerin birbirini ittiği karşıt yüklülerin birbirini çektiği ve bu çekim ya da itim kuvvetinin hesaplanması için gerekli denklemi de içeren kanunu bulmuştur.[27] Phlogiston teorisi 18. yüzyılın sonlarına gelindiğinde Lavoisier tarafından çürütülmüştür. Daha önceden Phlogiston teorisine göre de-phogiston maddesi olarak adlandıralan maddenin oksijen olduğunu keşfetmiştir.[28] 1803 yılında John Dalton atom teorisini kraliyet enstitünde ilk kez sunmuştur. Bu teoriye göre farklı elementlerin atomları, farklı ağırlıklara sahiptirler. Bu teorinin bazı ilkeleri;
Bütün maddeler atomlardan meydana gelmektedir.
Atomlar daha küçük parçalara ayrılamazlar.
Aynı elementin bütün atomları birbirinin aynısıdır.
Farklı elementler farklı atomlara sahiptir.
Atomların yeniden düzenlenmesi sonucu kimyasal tepkimeler meydana gelir.
Bileşikler elementlerden meydana gelirler.
şeklinde ifade edilebilinir.[29] Bu teoriyle modern kimyanın temelleri atılmış olur.
Modern kimya
Bu dönem 19. yüzyıl ve sonrasını kapsar. Heinrich Geißler (1814-1879) 1854 yılında suyun en yüksek yoğunluğa 3.8 C° ulaştığını kendi icat ettiği bir mekanizmayla göstermiştir (daha sonra bu sıcaklığın 3.98 C° olduğu bulunmuştur).[31] Daha sonra Geisslerin icat ettiği vakum tüpüyle William Crookes atom teorisinde ilerlemeler kaydetmiş ve Cathode ray'i keşfetmiştir.[32]
Eugene Goldstein(1850-1930)'ın çalışmaları protonun varlığını ispatlamıştır.J. J. Thomson (1856 1940) kendi atom modelini geliştirmiş ve 1906 yılında Nobel fizik ödülünü kazanmıştır.[33] Mendeleyev periyodik tabloyu 1869 yılında Kimyanın Prensipleri adlı eserinde yayımlamıştır. Bu periodik tabloda bilinen 63 elementi atom ağırlıklarına ve benzer özelliklerine göre sıralamıştır.[34] Marie Curie (1867 1934) radyoaktiviteyi ve sonrasında Polonyum ve Radyum'u keşetmiştir.[35] 1911 yılında Nobel kimya ödülünü kazanmıştır.[36] Ernest Rutherford 3 çeşit radyoaktifliği alfa parçacığı (+), beta parçacığı (-) ve gama ışınını keşfetmiştir.[37][38][39] Bu gelişmelerin sonrasında ve öncesinde daha birçok bilim insanının katkısıyla kimya bilimi günümüze ulaşmıştır. 2011 yılı Birleşmiş Milletler tarafından uluslararası kimya yılı ilan edilmiştir.
Temel kavramlar ve konular
Antik Yunanistan ve Antik Mısır'da belli başlı asitler ve bazlar hali hazırda sınıflandırılmışlardı.[41] Yunanlılar ekşimsi tad veren sirke gibi maddeleri ὀξύς (ekşi) olarak adlandırmışlar[42], daha sonra bu sözcük Latinceye acere olarak geçmiş[43] , ve Avrupa dillerindeki anlamı da latinceden türeyerek bu dillere geçmiştir. Oksijen elementinin adı da Antoine Lavoisier'in oksijeni (asid üreten anlamında) hatalı tanımlamasından kaynaklanmaktadır.[44] Asit ve bazların farklı tanımları mevcuttur.
Arheniusun tanımına göre;
Asit, suda çözüldüğünde çözeltiye H+ bırakan maddelerdir
Baz ise, OH- bırakan maddelerdir.[45]
Bronsted-Lowry tanımına göre;
Asit, proton (H+) bırakan maddelere denir.
Baz, proton kabul eden maddelerdir.[46]
Lewis Teorisine göre;
Asit, H+ iyonu gibi, çözeltiden elektron eksilten maddelerdir [47]
Baz ise, electron veren maddelerdir. Diğer tanımlardan farklı olarak sadece elektron alışverişi üzerine kurulmuş bir tanımlamadır.[48]
Asit-Baz tepkimeleri
Asit ve baz etkileşim halinde bırakıldıklarında, tuz üreterek bir diğerini nötrleştirme eğilimi gösterirler. HCl ve NaOH'ın tepkimesi NaCl bileşiği (tuz) ve su üretir.[49]
HCl + NaOH → NaCl + H2O
Atomun yapısı
1803-1808 yılları arasında öğretmenlik mesleğini yerine getirmekte olan John Dalton kimyanın iki temel yasası olan kütlenin korunumu ve sabit oranlar'ı kullanarak temel atom teorisini tanımlamıştır. Dalton'un atom teorisi üç ana önermeyi içermekteydi.[50] Bunlar;
Her kimyasal element küçük, bölünemeyen atom olarak adlandırılan parçacıklardan oluşmaktadır.
Aynı elementin atomları bir birine ağırlık ve özellikleri bakımından benzerdirler, fakat farklı elementlerin atomları birbirinden farklıdırlar.
Herhangi bir bileşik oluşurken, farklı elementler basit bir sayısal oranda birleşirler. Örneğin A atomu B atomuyla birleşip AB bileşiğini oluşturuyorsa, 2AB bileşiğini oluşturmak için 2A 2B'ile tepkimeye girmek zorundadır.[51]
Dalton'un atom teorisini tanımlamasından yaklaşık yüzyıl sonra atomun temel parçacıkları keşif edilmiştir. 1897 yılında elektron[52], 1909 yilinda proton[53] ve 1932 yilinda nötron[54] keşif edilmiştir.
Modern atom teorisi öncesi atom modelleri

Thomson'ın atom modeli
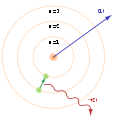
Bohr atom modeli
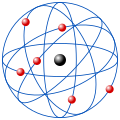
Rutherford atom modeli
Atom'un temel parçacıkları keşif edildikten sonraki dönemde birçok isim atom teorisine kayda değer katkılar sağlamıştır. Bu isimlerden bazıları Einstein, De Broglie, Schrodinger, ve Heisenberg'dir.
Kuantum teorisi elektronların parçacık olmakla birlikte, aynı zamanda dalga özelliklerine sahip olduğunu göstermiştir. Modern atom teorisine göre atom etrafı olasılık bulutlarıyla (orbital) çevrili atom çekirdeğinden oluşmaktadır. Bu olasılık bulutları da elektronların en olası bulundukları yerleri ifade etmektedir. Dalga denklemleri kullanılarak bu orbitallerin şekli ve büyüklüğü hesaplanabilmektedir.
Moleküllerin yapısı
Molekül bir birine bağlı bir grup atomun oluşturduğu kimyasal bileşiklerin en küçük temel yapısına verilen addır.[58] Diğer bir ifadeyle bir molekül bir bileşiği oluşturan atomların eşit oranlarda bulunduğu en küçük birimdir. Moleküller yapılarında birden fazla atom içerirler. Bir molekül aynı iki atomun bağlanması sonucu ya da farkı sayılarda farklı atomların bağlanması sonucu da oluşabilirler. Bir su molekülü 3 atomdan oluşur; iki hidrojen ve bir oksijen. Bir hidrojen peroksit molekülü iki hidrojen ve iki oksijen atomundan oluşur. Diğer taraftan bir kan proteini olan gamma globulin 19996 sayıda atomdan oluşmakla birlikte sadece 4 çeşit farklı atom içerir; hidrojen, karbon, oksijen ve nitrojen.[59] Molekülleri oluşturan kimyasal bağlara Moleküler bağlar denir. Bunlar kovalent, iyonik ve metalik bağlardır.
Moleküller arası kuvvetler
Moleküller arası kuvvetler, bir bileşiğin molekülleri arasında bulunan çekim kuvvetleridir. Bu kuvvetler bir bileşiğin katı, sıvı ya da gaz halinde bulunmasında, kaynama ve erime noktalarının değerinde ve çözünürlüğünde önemli rol oynar.[62] Moleküller arası kuvvetler Van der Waals kuvvetleri, ve hidrojen bağıdır.
Bileşikler
Su, amonyak, karbonmonoksit, ve karbondioksit gibi aşina olduğumuz maddeler aslında kimyasal bileşiktir. Bunların yanında daha az aşina olduğumuz sakkaroz (çay şekeri), asetilsalisilik asit (aspirin), ve askorbik asit (c vitamini) de kimyasal bileşiklere örnek teşkil etmektedirler. Bütün bu bileşiklerin ortak özelliği herbirinin iki ya da daha fazla elementten oluşuyor olmalarıdır. Öyleyse, kimyasal bileşik iki ya da daha elementin atomlarının oluşturduğu aynı özelliklere sahip moleküllerin oluşturduğu maddelerdir.[64] Kimyasal bileşikler moleküler bileşik ve iyonik bileşik olmak üzere ikiye ayrılır.
Bileşik çeşitleri
1.Moleküler Bileşik moleküllerden oluşmaktadır. Bu moleküller genel olarak metal olmayan birbirine kovalent bağla bağlı atomlardan oluşmaktadırlar. Moleküler Bileşikler kimyasal formüllerle ifade edilirler. Bu fomüller de bileşin içerdiği elementleri ve bu elementlerin birbirine orantılı sayılarını vermektedir. Formül çeşitleri;
Empirik formül molekül hakkında çok fazla bilgi vermemekle birlikte sadece elementlerin orantısal sayılarını vermektedir. Örneğin, CH2O empirik formülü hem C2H4O2 hem de C6H12O6 molekülleri için aynıdır.
Moleküler formül molekülü oluşturan elementlerin sayılarını vermektedir. C6H12O6 moleküler fomüle örnektir.
Yapısal formül ise molekülün içerisindeki bağlarıda göstermektedir.
2.İyonik Bileşik positiv ve negativ iyonların elektrostatik çekimle birleşimi sonucu oluşan bileşiklerdir.
Çözeltiler
Çözünürlük, bir maddenin bir solvent içerinde çözünme miktarını ifade etmek için kullanılır. Genelikle çözünen maddenin miktarının (solute) solventin hacmine bölünmesiyle elde edilir.[66] Çözünürlüğü etkiyen faktörler;
Sıcaklık
Cözen ve çözülen maddelerin doğası
Basınç
olarak sıralanabilinir.
Elektrokimya
Elektrokimya elektrik ve kimyasal değişimler arasındaki ilişkileri inceler. Kendiliğinden gelişen birçok kimyasal tepkime sonucunda elektrik akımı oluşmaktadır. Öte yandan elektrik akımı kendiliğinden gelişmeyen birçok tepkimenin gerçekleştirilmesinde kullanılmaktadır. Elektroliz süreciyle elektrik enerjisi kimyasal enerjiye dönüştürülebilmektedir.[68]
Kimyasal bağlar
Kimyasal bağ farklı atomların elektronlarının etkileşimi sonucu oluşur ve atomları bir arada tutar. Kimyasal bağ atomlar arası elektron alış verişi sonucu oluşuyorsa iyonik bağ, eğer ortak paylaşım sonucu oluşuyorsa kovalent bağ olarak adlandırılır. Elektronların metal atomları arasında paylaşımı sonucu oluşuyorsa da buna [Metalik bağ|metalik bağ] denir.[69]
Kinetik
Kimyasal kinetik, kimyasal tepkimeleri tepkime hızı, değişkenlerin tepkimeye etkileri, atomların yeniden dizilişi, ve ara ürünlerin oluşumu gibi açılardan ele alır.[70]
Stokiyometri
Stokiyometri, kimyasal bir tepkimede bulunan reaktanların ve ürünlerin miktarlarının bir birleriyle olan sayısal ilişkilerini inceler. Dengedeki bir kimyasal tepkime ifadesinde, katsayılar kaç mol reaktanın bir diğer bir reaktanla tepkimeye girmek için gerekli olduğunu ve bu tepkimeden kaç mol ürün elde edileceğini ortaya koymada kullanılan metoddur.[71] Dengede olan bir tepkimede reaktanların ve ürünlerin miktarları arasında bölen ve bölünen kısımlarında pozitif tam sayılar içeren bir orantı oluştumaktadır. Örneğin Metan'ın Oksijen'le tepkimesinde, 1 molekül Karbondioksit ve 2 molekül su oluşması için 1 molekül Metan 2 molekül oksijen ile tepkimeye girmelidir.[72]
CH4 + 202 → 1CO2 + 2H2O
Termodinamik
Termodinamik, enerji, ısı, entropi ve ekserji gibi fiziksel kavramlarla ilgilenen bilim dalı. Termodinamik her ne kadar sistemlerin madde ve/veya enerji alış-verişiyle ilgilense de, bu işlemlerin hızıyla ilgilenmez. Bundan dolayı aslında termodinamik denilirken, denge termodinamiği kastedilir. Zamana bağlı termodinamik olaylarla, denge halinde olmayan termodinamik ilgilenir.
Kimyanın temel kanunları
Avogadro yasası
Boyle yasası
Charles yasası
Gay-Lussac yasası
Enerjinin korunumu yasası
Kütlenin korunumu yasası
Dalton yasası
Sabit oranlar yasası
DulongPetit yasası
Faraday'ın elektroliz yasası
Gay-Lussac yasası
Graham difüzyon yasası
İdeal gaz yasası
Katlı oranlar yasası
Peryodik tablo yasası
Kimyanın ana bilim dalları
Kimya'nın ana alt dalları şöyle sıralanabilinir[73] ;
Analitik kimya
Anorganik kimya
Organik kimya
Fizikokimya
Termodinamik
Spektroskopi
Kimyasal kinetik
Teorik kimya
Kimya köken bilimi
Kimya sözcüğüyle simya sözcüğünün aynı kökten geldiği tahmin edilmektedir. 17 yüzyılda kimya ve simya sözcükleri aynı bilimsel disiplini, (maddenin analizi, sentezini içeren çalışmaları) tanımlamak için ayırt edilmeksizin kullanılmışlardır. Ancak 18. yüzyılda bu iki sözcük arasında bir ayrım gözetilmeye başlanmış, simya daha çok metalden altın yapmakla ilgili uğraşları tanımlamak için kullanılmıştır.[3] Simya sözcüğünün Arapça al-kimia (الكيمياء‎ sözcüğünden türediği[4], bu Arabça sözcüğünde Antik Yunanca himya (metal eritmek alnamına gelen χημεία ya da χημία sözcüğünden türediği idda edilmektedir
Tarih
Kimya'nın tarihi Simya öncesi, Simya dönemi, Geleneksel ve Modern kimya dönemleri olmak üzere 4 ana başlık altında toplanarak incelenebilinir.
Simya öncesi
Kimyanın bilinen tarihi Antik Mısır döneminde başlamıştır. MÖ 2000'li yıllarda Mısırlılar'ın kimyasal yöntemler kullanarak kosmetik tozlar ürettikleri idda edilmektedir.[6] Kral Hamurabi döneminde (MÖ 1792-1750) Babiller altın, gümüş, civa, kurşun, demir ve bakır gibi metalleri tanımlanmış ve bu metallere semboller verilmiştir.[7] Erken Yunan felsefeciler (Sokrates öncesi düşünürler) doğal olayları doğaüstü olmayan nedenlerle açıklamaya çalışmışlar[8], bunun sonucunda da bu dönemde simya öncesi kimya biliminin temelleri atılmıştır. Miletli Tales (MÖ 624 MÖ 546) maddenin presiplerini araştırmış ve suyun evrenin temel maddesi olduğunu öne sürmüştür.[9] Bir diğer Miletli Anaksimandros (MÖ 610- MÖ 546) suyun karşıtı olan ateşin nasıl oluştuğunu sorgulamıştır.[10] Empedokles (MÖ 490-430) evrenin 4 temel element ateş, hava, su ve topraktan oluştuğunu idda etmiştir.[11] Empedokles'in tanımına göre toprak katı maddeleri, su sıvı maddeleri ve metalleri, hava gasları ifade etmekteydi. Bununla beraber ateşide bir süreçten çok sıvı,gaz ve katı gibi maddenin bir hali olarak tanımlamıştır. Demokritos'un hocası Leukippos evrenin iki çeşit elementten oluştuğunu (boşluk ve katı) ifade etmiş, boşluğun ve katılığın evrendeki tüm elementleri oluşturduğunu ifade etmiştir.[12] Democritus (MÖ 460-370 ) Leukippos ile birlikte atomcu teoriyi geliştirmiştir.[13] Maddelerin yapı taşı olarak daha küçük parçalara ayrılamayan atomlar Leucippus ve Democritus'un geliştirdiği bir felsefe sistemi olarak kabul edilmesine rağmen Platon bu atomculuk teorisine bölünemezlik prensibini eklemiştir. Plato evreni oluşturan 4 temel elementin geometirik katılardan oluştuğunu bu katılarında üçgen yüzeylerden oluştuğunu idda etmiştir.[14] Aristoteles (MÖ 384-323) elementlerin özellikleri düşüncesini geliştirmiştir. Farklı elementlerin farklı özellikleri olduğunu ve bunun çeşitli nicel değişkenlere bağlı olduğunu ifade etmiştir. Bu nicel özellikleri değiştirildiğinde bir elementin başka bir elemente dönüştürülebileceğini ve maddelerin değişim halinde olduğunu idda etmiştir.
Simya dönemi
Aristotalesin fikirlerinden etkilenen simyacılar (yaklaşık MÖ 320, MS 300) yılları arasında Yunanca konuşulan akdeniz kıyılarında, Mısır'da, İran'da Aristotales ve diğer Yunan filozofların teorilerini pratiğe geçirmeye başlamışlardır.[16][17] Yine bu dönemde ilk defa simyacılar ucuz metallerden altın elde etmeyi mümkün kılması düşünülen felsefe taşını üretmeye çalışmışlardır.[7]
13. yüzyıla gelindiğinde simya tüm Avrupa kıtasında yaygın bir hale gelmiş, örneğin dönemin önemli bilim adamlarından Raymundus Lullus[18] İngiltere kralı tarafından İngiltere'ye basit metalden altın üretmesi için davet edilmiştir.[7] 13. yüzyılın başlarında dönemin ünlü simyacıları Roger Bacon[19] (1214/12201292), Albertus Magnus[20], ve Raymundus Lullus basit metalden altın üretme yöntemleri dışında simyanın diğer alanlarına yönelip, simyanın günümüz kimyasına yaklaşmasına öncü olmuşlardır.[21]
14. yüzyılda Katolik Kilisesi simya karşıtı taraf olmuş ve 1317 yılında Papa John XXII simyacılığı yasaklamıştır.[22]
17. yüzyıla gelindiğinde simya göreceli olarak az da olsa hala varlığını sürdürmekteydi. 17. yüzyılın etkin bilim adamlarından Robert Boyle 1661 yılında döneminde büyük yankı uyandıran eseri The Sceptical Chymist'i yayımlamıştır.[23] Aristotales'in 4 element teorisini ret eden bu kitap aynı zamanda simyanın döneminin de sona erdiğini işaret etmekteydi.[24]
Simya döneminde simyacıların araştırmaları ve deneyleri vasıtasıyla birçok laboratuvar tekniği geliştirilmiş ve çeşitli bileşik ve elementler keşif edilmiştir
Geleneksel kimya
Bu dönem 17. yüzyıl sonuyla 19. yüzyıl başlarına denk gelmektedir. Johann Joachim Becher 17. yüzyıl ortalarında yanma ile ilgili Phlogiston teorisini geliştirmiştir. Bu teoriye göre her yanıcı madde phlogiston diye adlandırılan kokusuz, renksiz, tatsız ve ağırlıksız bir içerik içermekteydi ve bu içerik yanma gerçekleştiğinde yanıcı madde tarafından ortama salınmaktaydı.[25]
Bu teori daha sonra Georg Ernst Stahl tarafından daha popüler bir hale getirilmiş 18. yüzyılın büyük bir kısmında genel kabül görmüştür.[26] 1785 1787 yılları arasında Fransız fizikçi Charles Augustine de Coulomb günümüzde Coulomb yasası olarak adlandırılan benzer yüklü maddelerin birbirini ittiği karşıt yüklülerin birbirini çektiği ve bu çekim ya da itim kuvvetinin hesaplanması için gerekli denklemi de içeren kanunu bulmuştur.[27] Phlogiston teorisi 18. yüzyılın sonlarına gelindiğinde Lavoisier tarafından çürütülmüştür. Daha önceden Phlogiston teorisine göre de-phogiston maddesi olarak adlandıralan maddenin oksijen olduğunu keşfetmiştir.[28] 1803 yılında John Dalton atom teorisini kraliyet enstitünde ilk kez sunmuştur. Bu teoriye göre farklı elementlerin atomları, farklı ağırlıklara sahiptirler. Bu teorinin bazı ilkeleri;
Bütün maddeler atomlardan meydana gelmektedir.
Atomlar daha küçük parçalara ayrılamazlar.
Aynı elementin bütün atomları birbirinin aynısıdır.
Farklı elementler farklı atomlara sahiptir.
Atomların yeniden düzenlenmesi sonucu kimyasal tepkimeler meydana gelir.
Bileşikler elementlerden meydana gelirler.
şeklinde ifade edilebilinir.[29] Bu teoriyle modern kimyanın temelleri atılmış olur.
Modern kimya
Bu dönem 19. yüzyıl ve sonrasını kapsar. Heinrich Geißler (1814-1879) 1854 yılında suyun en yüksek yoğunluğa 3.8 C° ulaştığını kendi icat ettiği bir mekanizmayla göstermiştir (daha sonra bu sıcaklığın 3.98 C° olduğu bulunmuştur).[31] Daha sonra Geisslerin icat ettiği vakum tüpüyle William Crookes atom teorisinde ilerlemeler kaydetmiş ve Cathode ray'i keşfetmiştir.[32]
Eugene Goldstein(1850-1930)'ın çalışmaları protonun varlığını ispatlamıştır.J. J. Thomson (1856 1940) kendi atom modelini geliştirmiş ve 1906 yılında Nobel fizik ödülünü kazanmıştır.[33] Mendeleyev periyodik tabloyu 1869 yılında Kimyanın Prensipleri adlı eserinde yayımlamıştır. Bu periodik tabloda bilinen 63 elementi atom ağırlıklarına ve benzer özelliklerine göre sıralamıştır.[34] Marie Curie (1867 1934) radyoaktiviteyi ve sonrasında Polonyum ve Radyum'u keşetmiştir.[35] 1911 yılında Nobel kimya ödülünü kazanmıştır.[36] Ernest Rutherford 3 çeşit radyoaktifliği alfa parçacığı (+), beta parçacığı (-) ve gama ışınını keşfetmiştir.[37][38][39] Bu gelişmelerin sonrasında ve öncesinde daha birçok bilim insanının katkısıyla kimya bilimi günümüze ulaşmıştır. 2011 yılı Birleşmiş Milletler tarafından uluslararası kimya yılı ilan edilmiştir.
Temel kavramlar ve konular
Antik Yunanistan ve Antik Mısır'da belli başlı asitler ve bazlar hali hazırda sınıflandırılmışlardı.[41] Yunanlılar ekşimsi tad veren sirke gibi maddeleri ὀξύς (ekşi) olarak adlandırmışlar[42], daha sonra bu sözcük Latinceye acere olarak geçmiş[43] , ve Avrupa dillerindeki anlamı da latinceden türeyerek bu dillere geçmiştir. Oksijen elementinin adı da Antoine Lavoisier'in oksijeni (asid üreten anlamında) hatalı tanımlamasından kaynaklanmaktadır.[44] Asit ve bazların farklı tanımları mevcuttur.
Arheniusun tanımına göre;
Asit, suda çözüldüğünde çözeltiye H+ bırakan maddelerdir
Baz ise, OH- bırakan maddelerdir.[45]
Bronsted-Lowry tanımına göre;
Asit, proton (H+) bırakan maddelere denir.
Baz, proton kabul eden maddelerdir.[46]
Lewis Teorisine göre;
Asit, H+ iyonu gibi, çözeltiden elektron eksilten maddelerdir [47]
Baz ise, electron veren maddelerdir. Diğer tanımlardan farklı olarak sadece elektron alışverişi üzerine kurulmuş bir tanımlamadır.[48]
Asit-Baz tepkimeleri
Asit ve baz etkileşim halinde bırakıldıklarında, tuz üreterek bir diğerini nötrleştirme eğilimi gösterirler. HCl ve NaOH'ın tepkimesi NaCl bileşiği (tuz) ve su üretir.[49]
HCl + NaOH → NaCl + H2O
Atomun yapısı
1803-1808 yılları arasında öğretmenlik mesleğini yerine getirmekte olan John Dalton kimyanın iki temel yasası olan kütlenin korunumu ve sabit oranlar'ı kullanarak temel atom teorisini tanımlamıştır. Dalton'un atom teorisi üç ana önermeyi içermekteydi.[50] Bunlar;
Her kimyasal element küçük, bölünemeyen atom olarak adlandırılan parçacıklardan oluşmaktadır.
Aynı elementin atomları bir birine ağırlık ve özellikleri bakımından benzerdirler, fakat farklı elementlerin atomları birbirinden farklıdırlar.
Herhangi bir bileşik oluşurken, farklı elementler basit bir sayısal oranda birleşirler. Örneğin A atomu B atomuyla birleşip AB bileşiğini oluşturuyorsa, 2AB bileşiğini oluşturmak için 2A 2B'ile tepkimeye girmek zorundadır.[51]
Dalton'un atom teorisini tanımlamasından yaklaşık yüzyıl sonra atomun temel parçacıkları keşif edilmiştir. 1897 yılında elektron[52], 1909 yilinda proton[53] ve 1932 yilinda nötron[54] keşif edilmiştir.
Modern atom teorisi öncesi atom modelleri

Thomson'ın atom modeli

Bohr atom modeli

Rutherford atom modeli
Atom'un temel parçacıkları keşif edildikten sonraki dönemde birçok isim atom teorisine kayda değer katkılar sağlamıştır. Bu isimlerden bazıları Einstein, De Broglie, Schrodinger, ve Heisenberg'dir.
Kuantum teorisi elektronların parçacık olmakla birlikte, aynı zamanda dalga özelliklerine sahip olduğunu göstermiştir. Modern atom teorisine göre atom etrafı olasılık bulutlarıyla (orbital) çevrili atom çekirdeğinden oluşmaktadır. Bu olasılık bulutları da elektronların en olası bulundukları yerleri ifade etmektedir. Dalga denklemleri kullanılarak bu orbitallerin şekli ve büyüklüğü hesaplanabilmektedir.
Moleküllerin yapısı
Molekül bir birine bağlı bir grup atomun oluşturduğu kimyasal bileşiklerin en küçük temel yapısına verilen addır.[58] Diğer bir ifadeyle bir molekül bir bileşiği oluşturan atomların eşit oranlarda bulunduğu en küçük birimdir. Moleküller yapılarında birden fazla atom içerirler. Bir molekül aynı iki atomun bağlanması sonucu ya da farkı sayılarda farklı atomların bağlanması sonucu da oluşabilirler. Bir su molekülü 3 atomdan oluşur; iki hidrojen ve bir oksijen. Bir hidrojen peroksit molekülü iki hidrojen ve iki oksijen atomundan oluşur. Diğer taraftan bir kan proteini olan gamma globulin 19996 sayıda atomdan oluşmakla birlikte sadece 4 çeşit farklı atom içerir; hidrojen, karbon, oksijen ve nitrojen.[59] Molekülleri oluşturan kimyasal bağlara Moleküler bağlar denir. Bunlar kovalent, iyonik ve metalik bağlardır.
Moleküller arası kuvvetler
Moleküller arası kuvvetler, bir bileşiğin molekülleri arasında bulunan çekim kuvvetleridir. Bu kuvvetler bir bileşiğin katı, sıvı ya da gaz halinde bulunmasında, kaynama ve erime noktalarının değerinde ve çözünürlüğünde önemli rol oynar.[62] Moleküller arası kuvvetler Van der Waals kuvvetleri, ve hidrojen bağıdır.
Bileşikler
Su, amonyak, karbonmonoksit, ve karbondioksit gibi aşina olduğumuz maddeler aslında kimyasal bileşiktir. Bunların yanında daha az aşina olduğumuz sakkaroz (çay şekeri), asetilsalisilik asit (aspirin), ve askorbik asit (c vitamini) de kimyasal bileşiklere örnek teşkil etmektedirler. Bütün bu bileşiklerin ortak özelliği herbirinin iki ya da daha fazla elementten oluşuyor olmalarıdır. Öyleyse, kimyasal bileşik iki ya da daha elementin atomlarının oluşturduğu aynı özelliklere sahip moleküllerin oluşturduğu maddelerdir.[64] Kimyasal bileşikler moleküler bileşik ve iyonik bileşik olmak üzere ikiye ayrılır.
Bileşik çeşitleri
1.Moleküler Bileşik moleküllerden oluşmaktadır. Bu moleküller genel olarak metal olmayan birbirine kovalent bağla bağlı atomlardan oluşmaktadırlar. Moleküler Bileşikler kimyasal formüllerle ifade edilirler. Bu fomüller de bileşin içerdiği elementleri ve bu elementlerin birbirine orantılı sayılarını vermektedir. Formül çeşitleri;
Empirik formül molekül hakkında çok fazla bilgi vermemekle birlikte sadece elementlerin orantısal sayılarını vermektedir. Örneğin, CH2O empirik formülü hem C2H4O2 hem de C6H12O6 molekülleri için aynıdır.
Moleküler formül molekülü oluşturan elementlerin sayılarını vermektedir. C6H12O6 moleküler fomüle örnektir.
Yapısal formül ise molekülün içerisindeki bağlarıda göstermektedir.
2.İyonik Bileşik positiv ve negativ iyonların elektrostatik çekimle birleşimi sonucu oluşan bileşiklerdir.
Çözeltiler
Çözünürlük, bir maddenin bir solvent içerinde çözünme miktarını ifade etmek için kullanılır. Genelikle çözünen maddenin miktarının (solute) solventin hacmine bölünmesiyle elde edilir.[66] Çözünürlüğü etkiyen faktörler;
Sıcaklık
Cözen ve çözülen maddelerin doğası
Basınç
olarak sıralanabilinir.
Elektrokimya
Elektrokimya elektrik ve kimyasal değişimler arasındaki ilişkileri inceler. Kendiliğinden gelişen birçok kimyasal tepkime sonucunda elektrik akımı oluşmaktadır. Öte yandan elektrik akımı kendiliğinden gelişmeyen birçok tepkimenin gerçekleştirilmesinde kullanılmaktadır. Elektroliz süreciyle elektrik enerjisi kimyasal enerjiye dönüştürülebilmektedir.[68]
Kimyasal bağlar
Kimyasal bağ farklı atomların elektronlarının etkileşimi sonucu oluşur ve atomları bir arada tutar. Kimyasal bağ atomlar arası elektron alış verişi sonucu oluşuyorsa iyonik bağ, eğer ortak paylaşım sonucu oluşuyorsa kovalent bağ olarak adlandırılır. Elektronların metal atomları arasında paylaşımı sonucu oluşuyorsa da buna [Metalik bağ|metalik bağ] denir.[69]
Kinetik
Kimyasal kinetik, kimyasal tepkimeleri tepkime hızı, değişkenlerin tepkimeye etkileri, atomların yeniden dizilişi, ve ara ürünlerin oluşumu gibi açılardan ele alır.[70]
Stokiyometri
Stokiyometri, kimyasal bir tepkimede bulunan reaktanların ve ürünlerin miktarlarının bir birleriyle olan sayısal ilişkilerini inceler. Dengedeki bir kimyasal tepkime ifadesinde, katsayılar kaç mol reaktanın bir diğer bir reaktanla tepkimeye girmek için gerekli olduğunu ve bu tepkimeden kaç mol ürün elde edileceğini ortaya koymada kullanılan metoddur.[71] Dengede olan bir tepkimede reaktanların ve ürünlerin miktarları arasında bölen ve bölünen kısımlarında pozitif tam sayılar içeren bir orantı oluştumaktadır. Örneğin Metan'ın Oksijen'le tepkimesinde, 1 molekül Karbondioksit ve 2 molekül su oluşması için 1 molekül Metan 2 molekül oksijen ile tepkimeye girmelidir.[72]
CH4 + 202 → 1CO2 + 2H2O
Termodinamik
Termodinamik, enerji, ısı, entropi ve ekserji gibi fiziksel kavramlarla ilgilenen bilim dalı. Termodinamik her ne kadar sistemlerin madde ve/veya enerji alış-verişiyle ilgilense de, bu işlemlerin hızıyla ilgilenmez. Bundan dolayı aslında termodinamik denilirken, denge termodinamiği kastedilir. Zamana bağlı termodinamik olaylarla, denge halinde olmayan termodinamik ilgilenir.
Kimyanın temel kanunları
Avogadro yasası
Boyle yasası
Charles yasası
Gay-Lussac yasası
Enerjinin korunumu yasası
Kütlenin korunumu yasası
Dalton yasası
Sabit oranlar yasası
DulongPetit yasası
Faraday'ın elektroliz yasası
Gay-Lussac yasası
Graham difüzyon yasası
İdeal gaz yasası
Katlı oranlar yasası
Peryodik tablo yasası
Kimyanın ana bilim dalları
Kimya'nın ana alt dalları şöyle sıralanabilinir[73] ;
Analitik kimya
Anorganik kimya
Organik kimya
Fizikokimya
Termodinamik
Spektroskopi
Kimyasal kinetik
Teorik kimya
